2.2.1氧气的性质(课时作业)
基础练习
1.关于氧气的物理性质的叙述,不正确的是( )
A.通常状况下,氧气是没有颜色、没有气味的气体
B.氧气不易溶于水
C.标准状况下,氧气的密度比空气的略大
D.液态氧和固态氧都是无色的
2. 下列关于氧气的化学性质和用途的说法正确的是( )
A.氧气能助燃,可作燃料
B.红磷能在空气中燃烧,产生大量的白色烟雾
C.细铁丝在空气中可剧烈燃烧,火星四射
D.氧气是一种化学性质比较活泼的气体,在一定条件下可与多种物质发生化学反应
3.为了区分一瓶氧气和一瓶空气,下列方案不可行的是( )
A.分别伸入带火星的木条,能复燃的是氧气
B.分别伸入被引燃的硫黄,产生明亮的蓝紫色火焰的是氧气
C.分别滴加澄清石灰水,无明显现象的是氧气
D.分别伸入燃着的木条,燃烧更剧烈的是氧气
4.小明同学在做铁丝在氧气中燃烧的实验时,用一根纱窗上的细铁丝在自己收集的氧气中进行实验,结果没有观察到 火星四射的现象。造成实验失败的原因不可能是
A.收集到的氧气量太少或纯度太低
B.铁丝表面的铁锈未除干净
C.集气瓶底没有铺一层细沙
D.铁丝末端火柴梗燃烧正旺,就将铁丝伸入集气瓶中
5.要将一充满空气的集气瓶中的氧气通过燃烧法除去,得到较为纯净的氮气,下列物质最合适的是 ( )
A.木炭B.硫黄C.红磷D.铁丝
能力提升
6.分析硫、木炭、铁丝三种物质在氧气中的燃烧,回答有关问题。
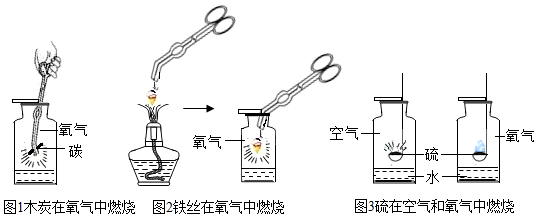
(1)从操作角度:三种可燃物都要自上而下______伸入氧气瓶中,铁丝燃烧实验中,需要在火柴快要燃尽时再伸入充满氧气的集气瓶中,其目的是______;集气瓶里放入少量水的作用是______。
(2)从现象角度:木炭在氧气中比在空气中燃烧得更旺:铁丝在空气中不燃烧,在氧气中才能剧烈燃烧,现象为______;在空气中点燃硫时,观察到淡黄色固体熔化后,燃烧发出淡蓝色火焰,在氧气中,燃烧得更旺,发出蓝紫色火焰。影响它们燃烧剧烈程度的因素是______,从微观角度解释该现象的原因是______。
(3)从反应角度:图2、图3三个反应有多个共同点______、______。(任意答2个)。
7.同学们在学习完氧气的性质后,知道了“氧气能使带火星的木条复燃”,在此基础上,同学们提出了以下问题,并逐一进行了探究。
(1)[问题一] 带火星的木条复燃能否证明气体是纯氧?
[进行实验] 同学们用数字化实验探测仪进行实验,并获得了一系列数据。
集气瓶编号 | ① | ② | ③ | ④ | ⑤ |
氧气浓度(体积分数) | 25% | 35% | 45% | …… | 65% |
带火星木条情况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
[收集证据] ④号集气瓶内的氧气浓度可能是 。
[实验结论] 。
(2)[问题二] 铁丝在氧气中的燃烧与氧气浓度和铁丝粗细有关系吗?
[收集证据]
实验编号 | 氧气浓度(体积分数) | 直径0.2 mm的细铁丝 | 直径0.5 mm的粗铁丝 |
① | 34% | 不燃烧 | 不燃烧 |
② | 47% | 稍有燃烧 | 不燃烧 |
③ | 60% | 剧烈燃烧 | 不燃烧 |
④ | 73% | 剧烈燃烧 | 稍有燃烧 |
⑤ | 86% | 剧烈燃烧 | 剧烈燃烧 |
[实验结论]
Ⅰ.氧气浓度越大,铁丝燃烧越 。
Ⅱ. 。
[反思与评价]
Ⅰ.探究铁丝粗细与燃烧剧烈程度的关系时,除了氧气浓度相同外,还需要 和 等条件也相同。
Ⅱ.在完成铁丝燃烧的实验时,为了保证实验成功,对于铁丝注意的事项是 。
参考答案
- D
2.D [解析] 氧气能助燃,但不具有可燃性,不可作燃料;红磷在空气中燃烧,产生大量的白烟,而不是白色烟雾;细铁丝在空气中不能燃烧。
3.C
4.C【详解】A、铁丝在空气中不燃烧,而空气中氧气的体积分数占21%,故在氧气量太少或纯度太低时,铁丝不能燃烧,不符合题意;
B、铁丝燃烧是铁与氧气的反应,如果铁丝表面有铁锈,则已被氧化,故不能再燃烧,不符合题意;
C、细沙是为了保护集气瓶底部不被高温生成物炸裂,与铁丝是否燃烧没有关系,符合题意;
D、为防止火柴梗燃烧消耗氧气瓶中的氧气,待铁丝末端火柴梗快燃尽时,再将铁丝伸入集气瓶中,否则火柴燃烧,消耗了氧气,会导致铁丝不能燃烧,不符合题意。故选C。
5.C [解析] 木炭和硫黄在空气中燃烧均生成气体,铁丝在空气中无法燃烧。
6(1) 缓慢 防止火柴消耗氧气 防止铁燃烧形成的高温熔融物溅落,炸裂集气瓶底
(2) 剧烈燃烧,火星四射,放热,生成黑色固体 氧气浓度 单位体积内氧分子和微粒接触的个数不同
(3) 都是化合反应 都有氧气参加反应、生成物都是氧化物等
【解析】(1)为防止氧气逸出装置,可燃物要缓慢通入氧气瓶中,故三种可燃物都要自上而下缓慢伸入氧气瓶中;故填:缓慢;
火柴会消耗集气瓶中的氧气,使氧气减少,故铁丝燃烧实验中,需要在火柴快要燃尽时再伸入充满氧气的集气瓶中,其目的是:防止火柴消耗氧气;
铁丝在氧气中点燃放出大量热,生成高温熔融物四氧化三铁,故集气瓶里放入少量水的作用是:防止铁燃烧形成的高温熔融物溅落,炸裂集气瓶底;
(2)物质燃烧只有当氧气浓度达到一定量,才能燃烧,氧气浓度较大时,物质燃烧更剧烈,铁丝在空气中不燃烧,在氧气中才能剧烈燃烧,现象为:剧烈燃烧,火星四射,放热,生成黑色固体;
在空气中点燃硫时,观察到淡黄色固体熔化后,燃烧发出淡蓝色火焰,在氧气中,燃烧得更旺,发出蓝紫色火焰。影响它们燃烧剧烈程度的因素是:氧气浓度;
氧气浓度较大时,单位体积内氧分子和微粒接触的数目不同,则从微观角度解释该现象的原因是:单位体积内氧分子和硫原子接触个数不同;
(3)
图2反应为铁在氧气中点燃生成四氧化三铁,图3反应为硫在氧气中点燃生成二氧化硫,则图2、图3反应均符合多变一,属于化合反应,都与氧气反应,生成物均由两种元素组成,其中一种元素均为氧元素,则生成物均为氧化物,故三个反应共同点:都是化合反应、都有氧气参加反应、生成物都是氧化物等。
7.(1)[收集证据] 55%
[实验结论] 带火星的木条复燃不能证明气体是纯氧
(2)[实验结论] Ⅰ.剧烈
Ⅱ.铁丝越细,燃烧越剧烈
[反思与评价] Ⅰ.集气瓶大小 铁丝长短(或引燃方式等,合理即可)
Ⅱ.铁丝需要打磨除去铁锈(或铁丝要盘成螺旋状并在下端系一根火柴)
[解析] (1)根据表格中的氧气的浓度数据每个间隔10%,可知④号集气瓶内的氧气浓度可能是55%,根据实验数据可得出结论:带火星的木条复燃不能证明气体是纯氧。